《人教版九年級(jí)化學(xué)下冊(cè) 第九單元溶液 溶解度曲線的應(yīng)用專題練習(xí)題及答案》由會(huì)員分享�,可在線閱讀�,更多相關(guān)《人教版九年級(jí)化學(xué)下冊(cè) 第九單元溶液 溶解度曲線的應(yīng)用專題練習(xí)題及答案(5頁珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�。
1、人教版九年級(jí)化學(xué)下冊(cè) 第九單元 溶液
溶解度曲線的應(yīng)用 專題練習(xí)題
訓(xùn)練題型1 溶解度曲線表示的意義
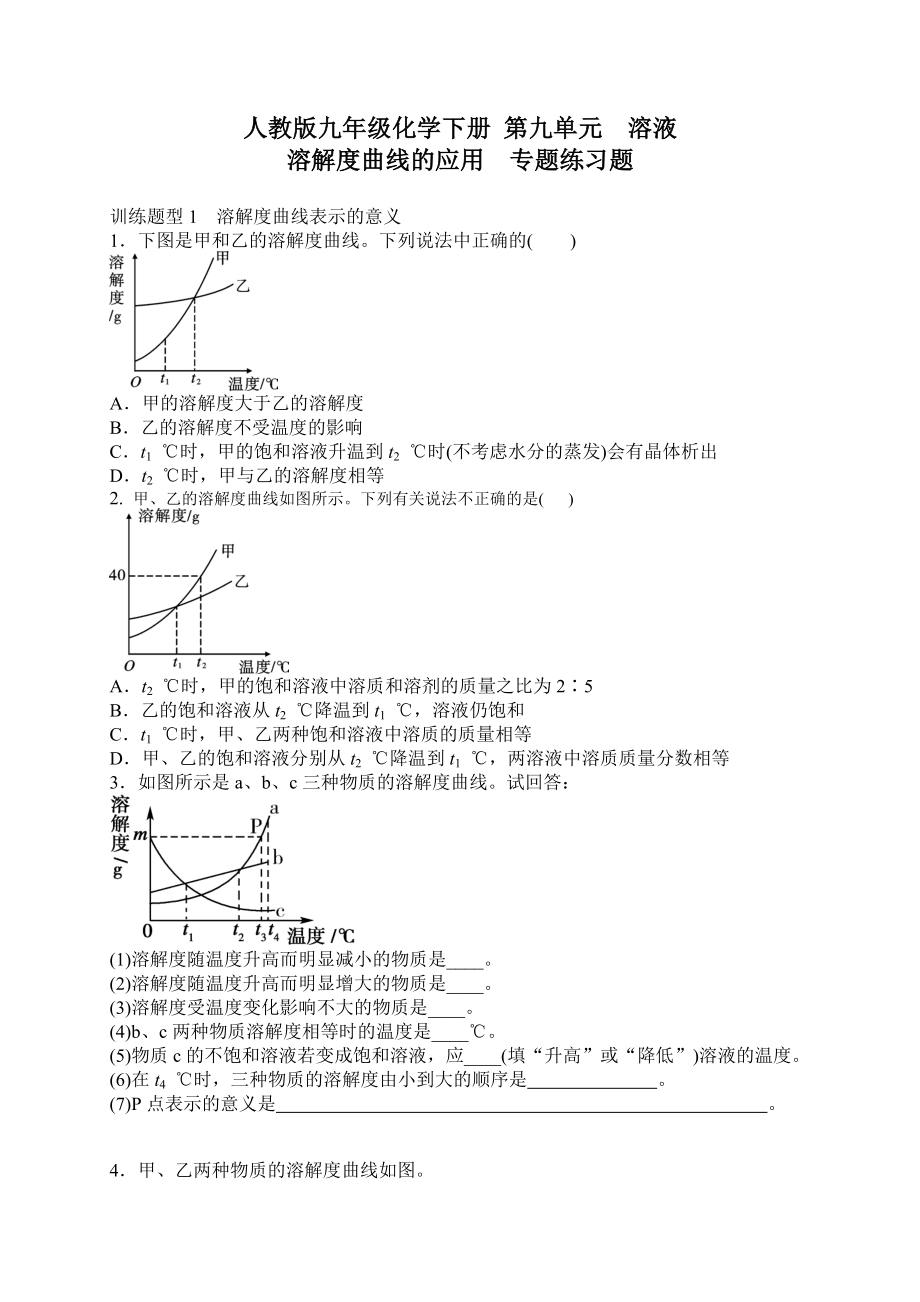
1.下圖是甲和乙的溶解度曲線�。下列說法中正確的( )
A.甲的溶解度大于乙的溶解度
B.乙的溶解度不受溫度的影響
C.t1 ℃時(shí),甲的飽和溶液升溫到t2 ℃時(shí)(不考慮水分的蒸發(fā))會(huì)有晶體析出
D.t2 ℃時(shí)�,甲與乙的溶解度相等
2. 甲、乙的溶解度曲線如圖所示�。下列有關(guān)說法不正確的是( )
A.t2 ℃時(shí),甲的飽和溶液中溶質(zhì)和溶劑的質(zhì)量之比為2∶5
B.乙的飽和溶液從t2 ℃降溫到t1 ℃�,溶液仍飽和
C.t1 ℃時(shí),甲�、乙兩種
2、飽和溶液中溶質(zhì)的質(zhì)量相等
D.甲�、乙的飽和溶液分別從t2 ℃降溫到t1 ℃,兩溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)相等
3.如圖所示是a�、b、c三種物質(zhì)的溶解度曲線�。試回答:
(1)溶解度隨溫度升高而明顯減小的物質(zhì)是____。
(2)溶解度隨溫度升高而明顯增大的物質(zhì)是____�。
(3)溶解度受溫度變化影響不大的物質(zhì)是____。
(4)b�、c兩種物質(zhì)溶解度相等時(shí)的溫度是____℃�。
(5)物質(zhì)c的不飽和溶液若變成飽和溶液,應(yīng)____(填“升高”或“降低”)溶液的溫度�。
(6)在t4 ℃時(shí)�,三種物質(zhì)的溶解度由小到大的順序是 �。
(7)P點(diǎn)表示的意義是
3、 �。
4.甲、乙兩種物質(zhì)的溶解度曲線如圖�。
(1)10 ℃時(shí),甲物質(zhì)的溶解度____(填“大于”“小于”或“等于”)乙物質(zhì)的溶解度�。
(2)40 ℃時(shí),把40 g甲物質(zhì)放入100 g水中�,所得的是 (填“飽和”或“不飽和”)溶液。
(3)20 ℃時(shí)�,甲物質(zhì)溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)不可能為____。
A.20% B.25% C.26.5% D.30%
訓(xùn)練題型2 溶解度曲線的應(yīng)用
5.三種固體物質(zhì)a�、b、c的溶解度曲線如圖所
4�、示,則下列說法不正確的是( )
A.t1 ℃時(shí)三種物質(zhì)的飽和溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)大小為b>a=c
B.a(chǎn)�、b、c三種物質(zhì)的飽和溶液從t2 ℃降溫到t1 ℃時(shí)都有晶體析出
C.t2 ℃時(shí)�,將50 g a物質(zhì)加入到100 g水中完全溶解形成飽和溶液
D.a(chǎn)中混有少量b時(shí)可采取降溫結(jié)晶的方法提純得到a
6. 如圖所示甲、乙�、丙三種物質(zhì)的溶解度曲線�,下列說法正確的是( )
A.t2 ℃時(shí),甲�、乙溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)一定相等
B.乙中含有少量甲�,可采用降溫結(jié)晶的方法提純乙
C.t3 ℃時(shí)�,甲、乙�、丙三種物質(zhì)的飽和溶液降溫到t1 ℃,所得溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)的
5�、大小關(guān)系為乙>丙>甲
D.t2 ℃時(shí),100 g甲的飽和溶液中加入400 g水�,得到10%的甲溶液
7. 如圖是甲、乙�、丙三種物質(zhì)的溶解度曲線,下列說法錯(cuò)誤的是( )
A.甲中混有少量雜質(zhì)乙�,可采用降溫結(jié)晶的方法進(jìn)行提純
B.t3 ℃時(shí),將甲�、丙的飽和溶液降溫,甲溶液溶質(zhì)的質(zhì)量分?jǐn)?shù)減小�,丙不變
C.t2 ℃時(shí),甲�、丙溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)甲>丙
D.t1 ℃時(shí),60 g水中溶解18 g甲可得到其飽和溶液
8. 下圖是甲�、乙兩種固體物質(zhì)的溶解度曲線。據(jù)圖回答:
(1)P點(diǎn)的含義是
6�、 。
(2)要使接近飽和的甲溶液變成飽和溶液�,
可采用的方法有 (寫出一種),當(dāng)甲中含有少量乙時(shí)�,
可采用 的方法提純甲。
(3)30 ℃ 時(shí)�,將40 g甲物質(zhì)放入盛有50 g水的燒杯中,所得溶液溶質(zhì)的質(zhì)量分?jǐn)?shù)為 �。若將燒杯內(nèi)物質(zhì)升溫到50 ℃(不考慮水蒸發(fā)),溶液中變化的是____(填序號(hào))�。
a.溶劑的質(zhì)量
b.溶液的質(zhì)量
c.溶質(zhì)的質(zhì)量分?jǐn)?shù)
(4)從圖中還可獲得的信息是
7、 �。(答出一條)
9. t1 ℃時(shí),將等質(zhì)量的硝酸鉀和氯化鉀分別加入到各盛有100 g水的兩個(gè)燒杯中�,充分?jǐn)嚢韬蟋F(xiàn)象如圖1所示,硝酸鉀和氯化鉀的溶解度曲線如圖2所示�。
(1)燒杯②中的上層清液是否達(dá)到飽和狀態(tài)?____(填“是”“否”或“無法判斷”)�;
(2)燒杯①中溶解的溶質(zhì)是 (寫名稱或化學(xué)式);
(3)將t1 ℃時(shí)50 g硝酸鉀的飽和溶液稀釋成10%的溶液�,需加水____g;
(4)關(guān)于圖中燒杯內(nèi)的物質(zhì)�,下列說法正確的是____。
A.燒杯①內(nèi)溶
8�、液中溶質(zhì)的質(zhì)量分?jǐn)?shù)>燒杯②內(nèi)上層清液中溶質(zhì)的質(zhì)量分?jǐn)?shù)
B.蒸發(fā)一定量的水,兩燒杯中都一定有固體析出
C.將兩個(gè)燒杯中的溶液混合�,充分?jǐn)嚢韬螅瑹幸欢ㄟ€有剩余固體
D.將溫度升高到t2 ℃�,兩燒杯內(nèi)溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)相等(不考慮水的蒸發(fā))
10. 如圖所示是甲、乙、丙三種固體物質(zhì)的溶解度曲線�。
(1)t2 ℃時(shí),甲�、乙、丙三種物質(zhì)的溶解度大小關(guān)系是 �;
(2)t1 ℃時(shí),50 g水中加入30 g的甲物質(zhì)充分溶解后�,可得到____g溶液�;
(3)下列說法正確的是(填序號(hào))____。
①t1 ℃時(shí)�,甲、丙兩溶
9�、液的溶質(zhì)質(zhì)量分?jǐn)?shù)一定相等
②t3 ℃時(shí)�,向100 g20%甲的溶液中加100 g水,充分?jǐn)嚢?,溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)為10%
③t2 ℃時(shí)�,升高丙溶液的溫度,一定有晶體析出
④t3 ℃時(shí)�,用等質(zhì)量的甲、乙�、丙分別配制成三種物質(zhì)的飽和溶液�,所需溶劑的質(zhì)量為甲<乙<丙
11. KNO3和NaCl在不同溫度時(shí)的溶解度如下表所示。請(qǐng)回答下列問題:
(1)依據(jù)上表數(shù)據(jù)�,繪制出KNO3和NaCl的溶解度曲線如圖�,圖中能表示KNO3溶解度曲線的是____(填“A”或“B”);
(2)由表中數(shù)據(jù)分析可知�,KNO3和NaCl在某一溫度時(shí)具有相同的溶解度�,則溫度的取值范圍是
10、 �;
(3)某興趣小組做了以下實(shí)驗(yàn):
上述實(shí)驗(yàn)過程中得到溶液一定屬于不飽和溶液的是 (填數(shù)字序號(hào))�,將⑤繼續(xù)冷卻至10 ℃,過濾�,共可回收得到KNO3固體____g�;
(4)硝酸鉀中含有少量氯化鈉時(shí),可通過 (填“蒸發(fā)結(jié)晶”或“降溫結(jié)晶”)的方法提純�。
答案:
1. D
2. C
3. (1)c (2) a (3) b
(4) t1 (5) 升高 (6) c<b<a (7) t3℃時(shí),a的溶解度為mg
4. (1) 小于 (2) 不飽和 (3) D
5. B
6. C
7. C
8. (1) 30℃時(shí)�,甲的溶解度為60g
(2) 降溫或加溶質(zhì) 冷卻熱飽和溶液
(3) 37.5% b、c
(4) t℃時(shí)�,甲�、乙溶解度相等
9. (1) 是 (2) 氯化鉀 (3) 50 (4) A
10. (1) 甲=乙>丙 (2) 60 (3) ②④
11. (1) A (2) 20℃~30℃ (3) ①③④ 59.1 (4) 降溫結(jié)晶
 人教版九年級(jí)化學(xué)下冊(cè) 第九單元溶液 溶解度曲線的應(yīng)用專題練習(xí)題及答案
人教版九年級(jí)化學(xué)下冊(cè) 第九單元溶液 溶解度曲線的應(yīng)用專題練習(xí)題及答案