《2022年高一化學(xué)第三章 第三節(jié)物質(zhì)的量濃度教學(xué)設(shè)計(jì) 人教版》由會(huì)員分享�,可在線閱讀�����,更多相關(guān)《2022年高一化學(xué)第三章 第三節(jié)物質(zhì)的量濃度教學(xué)設(shè)計(jì) 人教版(3頁珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
1����、2022年高一化學(xué)第三章 第三節(jié)物質(zhì)的量濃度教學(xué)設(shè)計(jì) 人教版
教學(xué)目標(biāo):
1�、知識(shí)與技能:會(huì)用物質(zhì)的量濃度這一物理量解決有關(guān)溶液組成的問題;會(huì)配制一定物質(zhì)的量濃度的溶液���。
2����、過程與方法:體會(huì)做中學(xué)的學(xué)習(xí)方式��,建立概念����;做的過程中善于利用資料���。
3、情感態(tài)度價(jià)值觀:學(xué)習(xí)從感性認(rèn)識(shí)上升到理性認(rèn)識(shí)的辯證唯物主義世界觀����,并用于指導(dǎo)實(shí)踐。
指導(dǎo)思想:應(yīng)用問題中心模式——任務(wù)驅(qū)動(dòng)教學(xué)����,設(shè)置真實(shí)情境,完成具體任務(wù)�,體驗(yàn)做中學(xué)建立概念,應(yīng)用概念解決實(shí)際問題����,體現(xiàn)新課程理念,為新課程實(shí)施進(jìn)行有益嘗試��。
教學(xué)重點(diǎn):物質(zhì)的量濃度概念的建立
教學(xué)難點(diǎn):設(shè)計(jì)實(shí)驗(yàn)配制一定體積的溶液
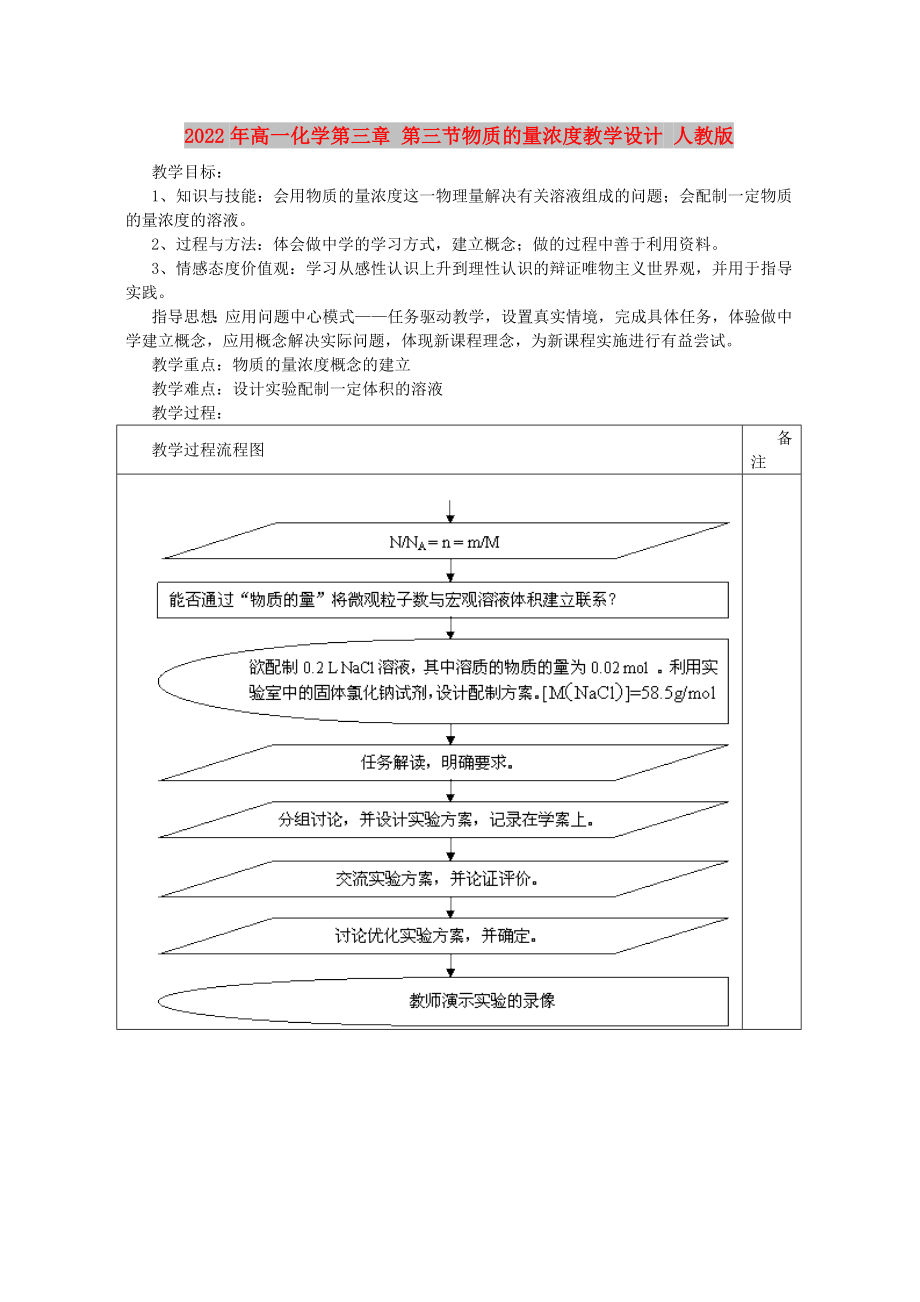
教學(xué)過程:
教學(xué)過
2��、程流程圖
備注
學(xué)習(xí)目標(biāo):
1�����、 進(jìn)一步認(rèn)識(shí)“物質(zhì)的量”是微觀粒子與宏觀物質(zhì)關(guān)系的橋梁,建立物質(zhì)的量濃度的概念�����,會(huì)寫其表達(dá)式���,能夠解決各量之間的轉(zhuǎn)化問題�����。
2�、 能夠按照要求完成配制一定體積的溶液的任務(wù)�����,并能表示其組成�����。
3�����、 體會(huì)“做中學(xué)”的學(xué)習(xí)方式�����,在設(shè)計(jì)實(shí)驗(yàn)方案和操作的過程中建立概念����。
4、 學(xué)習(xí)發(fā)現(xiàn)問題的方法����。
學(xué)習(xí)過程:
一、 復(fù)習(xí):怎樣通過“物質(zhì)的量”將微觀粒子數(shù)與宏觀物質(zhì)的質(zhì)量建立聯(lián)系����?
關(guān)系式:
二、“物質(zhì)的量濃度”概念的建立:
任務(wù):配制一定組成的溶液��,并表示其組成���。
現(xiàn)欲配制0.2 L
3�、NaCl溶液��,其中溶質(zhì)的物質(zhì)的量為0.02 mol ����。[M(NaCl)=58.5g/mol]請(qǐng)你利用實(shí)驗(yàn)室中的固體氯化鈉試劑�����,設(shè)計(jì)配制方案���。
請(qǐng)選擇實(shí)驗(yàn)儀器:
實(shí)驗(yàn)方案:
實(shí)驗(yàn)記錄:
請(qǐng)你與同學(xué)討論,為我們配制的溶液制作標(biāo)簽�����。
結(jié)論:物質(zhì)的量濃度:
1����、 表達(dá)式:
2、 單位:
3����、 定義:
活動(dòng)一——從上述溶液中取出10.0mL,取出了多少溶質(zhì)�����?(用多種方式表達(dá))
活動(dòng)二——從這張?bào)w檢化驗(yàn)單中你獲得了哪些信息?
活動(dòng)三——實(shí)驗(yàn)室已配好下列溶液待用�����,請(qǐng)為它們貼上標(biāo)簽:
A�����、將4gNaOH固體溶于水配成250mL溶液[M(NaOH)=40g/mol]��;
B����、將10.6gNa2CO3固體溶于水配成250mL溶液[M(Na2CO3)=106g/mol]。
活動(dòng)四——怎樣配制500mL0.4mol/L NaCl溶液? [M(NaCl)=58.5g/mol]
小結(jié):物質(zhì)的量將微粒數(shù)目與物質(zhì)的質(zhì)量����、溶液體積建立了怎樣的關(guān)系?
新任務(wù)
你對(duì)錄像中的實(shí)驗(yàn)操作過程有疑問嗎�?思考你的問題,下次課繼續(xù)研究�。
 2022年高一化學(xué)第三章 第三節(jié)物質(zhì)的量濃度教學(xué)設(shè)計(jì) 人教版
2022年高一化學(xué)第三章 第三節(jié)物質(zhì)的量濃度教學(xué)設(shè)計(jì) 人教版