《2022年高考化學(xué)一輪綜合復(fù)習(xí) 第6章 化學(xué)反應(yīng)與能量變化 課時(shí)4 新型化學(xué)電源題型沖關(guān)練習(xí)》由會(huì)員分享��,可在線閱讀����,更多相關(guān)《2022年高考化學(xué)一輪綜合復(fù)習(xí) 第6章 化學(xué)反應(yīng)與能量變化 課時(shí)4 新型化學(xué)電源題型沖關(guān)練習(xí)(3頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索。
1��、2022年高考化學(xué)一輪綜合復(fù)習(xí) 第6章 化學(xué)反應(yīng)與能量變化 課時(shí)4 新型化學(xué)電源題型沖關(guān)練習(xí)
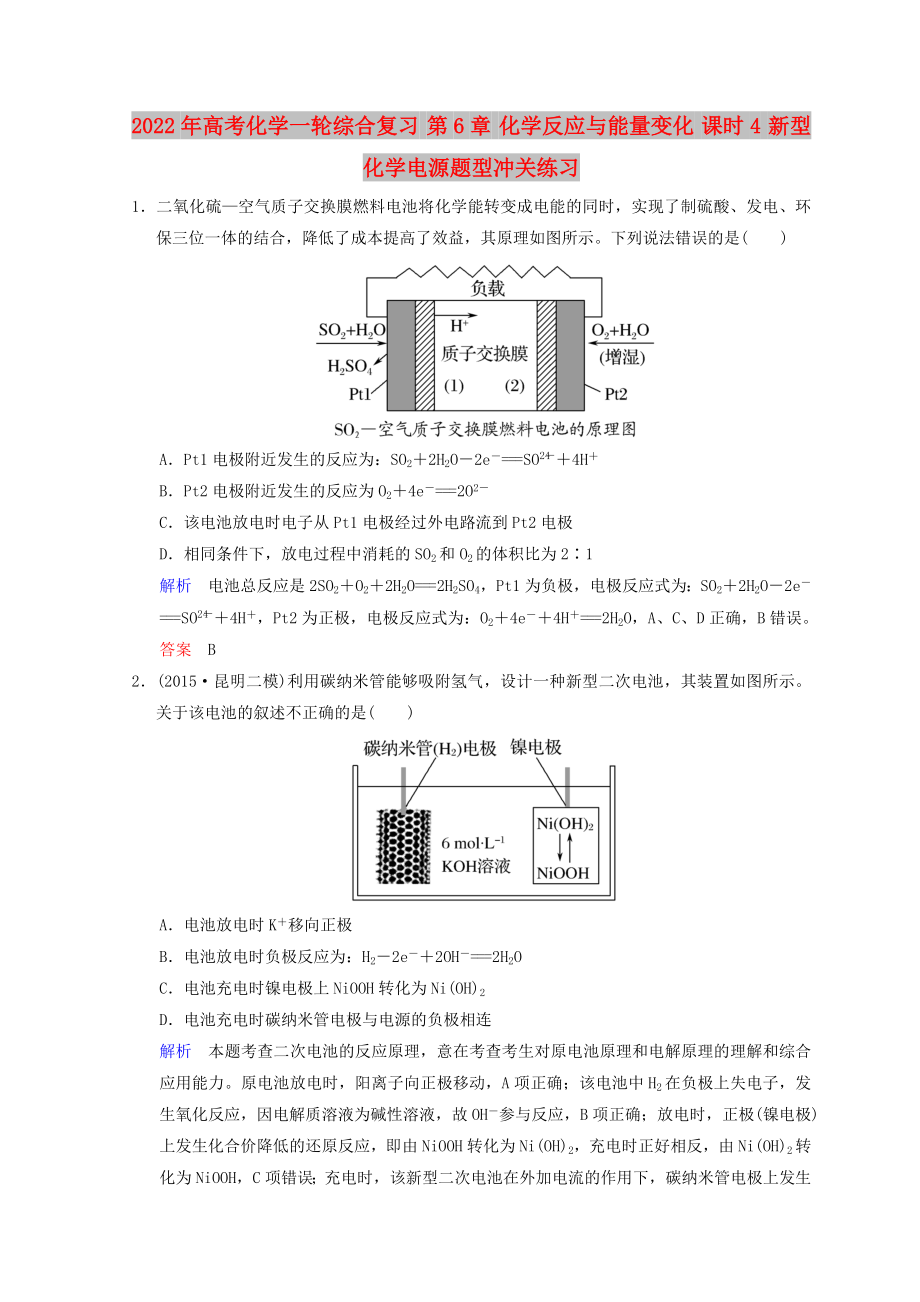
1.二氧化硫—空氣質(zhì)子交換膜燃料電池將化學(xué)能轉(zhuǎn)變成電能的同時(shí)���,實(shí)現(xiàn)了制硫酸、發(fā)電���、環(huán)保三位一體的結(jié)合�,降低了成本提高了效益,其原理如圖所示�。下列說(shuō)法錯(cuò)誤的是( )
A.Pt1電極附近發(fā)生的反應(yīng)為:SO2+2H2O-2e-===SO+4H+
B.Pt2電極附近發(fā)生的反應(yīng)為O2+4e-===2O2-
C.該電池放電時(shí)電子從Pt1電極經(jīng)過(guò)外電路流到Pt2電極
D.相同條件下,放電過(guò)程中消耗的SO2和O2的體積比為2∶1
解析 電池總反應(yīng)是2SO2+O2+2H2O===2H2SO4��,Pt1為
2����、負(fù)極,電極反應(yīng)式為:SO2+2H2O-2e-===SO+4H+����,Pt2為正極,電極反應(yīng)式為:O2+4e-+4H+===2H2O����,A、C��、D正確���,B錯(cuò)誤����。
答案 B
2.(2015·昆明二模)利用碳納米管能夠吸附氫氣���,設(shè)計(jì)一種新型二次電池����,其裝置如圖所示。關(guān)于該電池的敘述不正確的是( )
A.電池放電時(shí)K+移向正極
B.電池放電時(shí)負(fù)極反應(yīng)為:H2-2e-+2OH-===2H2O
C.電池充電時(shí)鎳電極上NiOOH轉(zhuǎn)化為Ni(OH)2
D.電池充電時(shí)碳納米管電極與電源的負(fù)極相連
解析 本題考查二次電池的反應(yīng)原理��,意在考查考生對(duì)原電池原理和電解原理的理解和綜合應(yīng)用能力����。原電池放電時(shí)
3、���,陽(yáng)離子向正極移動(dòng)��,A項(xiàng)正確��;該電池中H2在負(fù)極上失電子�,發(fā)生氧化反應(yīng)����,因電解質(zhì)溶液為堿性溶液,故OH-參與反應(yīng)��,B項(xiàng)正確����;放電時(shí),正極(鎳電極)上發(fā)生化合價(jià)降低的還原反應(yīng)��,即由NiOOH轉(zhuǎn)化為Ni(OH)2��,充電時(shí)正好相反���,由Ni(OH)2轉(zhuǎn)化為NiOOH����,C項(xiàng)錯(cuò)誤���;充電時(shí)���,該新型二次電池在外加電流的作用下,碳納米管電極上發(fā)生還原反應(yīng)�,故碳納米管電極作陰極,與電源負(fù)極相連���,D項(xiàng)正確��。
答案 C
3.(2016·臨沂質(zhì)檢)研究人員研制出一種可快速充放電的超性能鋁離子電池�,Al、Cn為電極����,有機(jī)陽(yáng)離子與陰離子(AlCl、Al2Cl)組成的離子液體為電解質(zhì)��。如圖為該電池放電過(guò)程示意圖���。下列說(shuō)法
4��、錯(cuò)誤的是( )
A.充電時(shí)��,Al做陰極���、Cn為陽(yáng)極
B.充電時(shí),每生成1 mol鋁�,同時(shí)消耗4 mol Al2Cl
C.放電時(shí),電解質(zhì)中的有機(jī)陽(yáng)離子向鋁電極方向移動(dòng)
D.放電時(shí)��,正極反應(yīng)式為Cn[AlCl4]+ e-=== Cn + AlCl
解析 由圖示知��,該電池放電時(shí)�,Al作負(fù)極,Cn作正極�,因此充電時(shí)����,Al做陰極����、Cn為陽(yáng)極��,A項(xiàng)正確����;充電時(shí),陰極反應(yīng)為4Al2Cl+3e-===Al+7AlCl���,B項(xiàng)正確��;放電時(shí)��,電解質(zhì)中的有機(jī)陽(yáng)離子向正電極方向移動(dòng)����,C項(xiàng)錯(cuò)誤���;放電時(shí)����,正極反應(yīng)式為Cn[AlCl4]+e-=== Cn+AlCl,D項(xiàng)正確���。
答案 C
4.(2016·長(zhǎng)
5����、沙一模)一種光化學(xué)電池的結(jié)構(gòu)如圖所示��,電池總反應(yīng)為:AgCl(s)+Cu+(aq)===Ag(s)+Cu2+(aq)+Cl-(aq)�,下列關(guān)于該電池在工作時(shí)的說(shuō)法中正確的是( )
A.生成108 g銀,轉(zhuǎn)移電子個(gè)數(shù)為1 mol
B.Cu+在負(fù)極發(fā)生氧化反應(yīng)
C.Ag電極活潑��,Ag失電子發(fā)生氧化反應(yīng)
D.Cl-由負(fù)極遷移到正極
解析 由題給反應(yīng)可知����,生成1 mol Ag,轉(zhuǎn)移1 mol e-�,即生成108 g Ag,轉(zhuǎn)移電子個(gè)數(shù)為NA�,A項(xiàng)錯(cuò)誤;負(fù)極Cu+失電子生成Cu2+�,化合價(jià)升高,發(fā)生氧化反應(yīng)���,B項(xiàng)正確���;Ag電極為正極�,AgCl得電子生成Ag和Cl-�,C項(xiàng)錯(cuò)誤��;Cl-由正極
6����、向負(fù)極遷移,D項(xiàng)錯(cuò)誤�。
答案 B
5.氨氣是一種富氫燃料,可以直接用于燃料電池��,下圖是供氨水式燃料電池工作原理:
(1)氨氣燃料電池的電解質(zhì)溶液最好選擇________(填“酸性”�、“堿性”或“中性”)溶液。
(2)空氣在進(jìn)入電池裝置前需要通過(guò)過(guò)濾器除去的氣體是
______________________________________________________________��。
(3)氨氣燃料電池的反應(yīng)是氨氣與氧氣生成一種常見(jiàn)的無(wú)毒氣體和水�,該電池的電極總反應(yīng)是________________,正極的電極反應(yīng)式是_________________________________________________________________�。
解析 氨氣為堿性氣體,會(huì)與CO2反應(yīng)����,由此可回答(1)(2)問(wèn)�。由信息和所含元素可知無(wú)毒氣體是氮?dú)?,在燃料電池中,燃料為?fù)極�,氧氣為正極,根據(jù)堿性環(huán)境可知��,正極反應(yīng)式為O2+4e- + 2H2O===4OH-�。
答案 (1)堿性 (2)CO2
(3)4NH3 + 3O2===2N2 + 6H2O 3O2+12e- + 6H2O===12OH-(或O2 + 4e- + 2H2O===4OH-)
 2022年高考化學(xué)一輪綜合復(fù)習(xí) 第6章 化學(xué)反應(yīng)與能量變化 課時(shí)4 新型化學(xué)電源題型沖關(guān)練習(xí)
2022年高考化學(xué)一輪綜合復(fù)習(xí) 第6章 化學(xué)反應(yīng)與能量變化 課時(shí)4 新型化學(xué)電源題型沖關(guān)練習(xí)